南京工大陈可泉:利用可再生原料生物合成脂肪族短链二元胺与醇的研究进展
绿色生物制造是以生物质等可再生原料通过生物过程和生物系统生产生物基材料、化学品、能源、医药和食品等,其绿色清洁的生产工艺有助于改善传统化工行业对化石资源高依赖以及工艺高能耗、高排放等问题。脂肪族短链二元胺和醇是重要的大宗化学品,可作为聚合单体应用于合成聚酯、聚氨酯、聚酰胺等高分子材料,同时在化妆品、制药等领域具有广泛应用。 【SynBioCon】获悉,近日,南京工业大学陈可泉教授团队在《化工进展》发表了《利用可再生原料生物合成脂肪族短链二元胺与醇的研究进展》,该文全面探讨了利用可再生原料生物合成1,3-丙二胺、1,4-丁二胺、1,5-戊二胺、1,3-丙二醇、1,4-丁二醇、1,5-戊二醇的研究进展,概况了可再生原料生物制造的碳循环和代谢途径,总结了脂肪族短链二元胺和二元醇的从头生物合成路线,阐述了利用木质纤维素水解糖、甘油、一碳化合物原料合成短链二元胺和醇的研究现状。并对脂肪族短链二元胺和醇生物制造主要面临的挑战进行了相关讨论和展望。
化工行业是国民经济中的重要组成,全球的精细化工产品种类已超10万种。以化石资源为原料的生产方式大量消耗石油、煤炭和天然气等不可再生资源,对资源储备带来了严重威胁,同时会大量排放CO2,造成环境污染。以可再生资源作为替代原料,发展绿色生物制造,有助于改善传统化工行业对化石资源高依赖,以及工艺高能耗、高排放等问题,对清洁、低碳、安全的环境有重要贡献。我国明确将生物基材料替代传统化学原料列入发展目标,对化石原料的替代已成为“向绿色低碳、无毒低毒、可持续发展模式转型”重要战略,“打造基于非粮生物质的生物基材料体系”是国家与行业发展的要求。脂肪族二元胺和二元醇分别是由两个氨基或两个羟基连接饱和烷基主链组成的大宗化学品,作为关键核心单体用于制造聚酯、聚氨酯、聚酰胺、聚醚多元醇等高分子材料,在工程塑料、涂料、纺织工业领域广泛应用,具有巨大的市场需求。
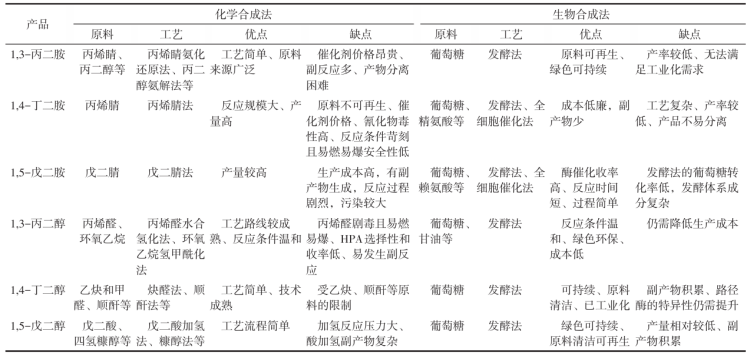
目前大多数二元胺和醇是由化石原料合成的,而生物合成二元胺和二元醇是“双碳”目标下的必然趋势。相较于化学合成二元胺和醇,生物合成具有明显的优势,见表1。
因此,涌现出大量的国内外科研机构和企业对此开展研究,并取得了显著的成果。目前,生物法合成1,3-丙二醇和1,4-丁二醇的技术分别经杜邦公司和美国Genomatica公司实现了商业化,并且与石油工艺相比,1,3-丙二醇生物合成工艺原料成本降低37%,同时可减少30%能耗和减排63%的CO2。针对生物基二元胺制备,宁夏伊品生物科技股份有限公司和上海凯赛生物产业有限公司采用全细胞催化法催化赖氨酸脱羧合成1,5-戊二胺,率先实现了1,5-戊二胺的规模化生产,凯赛宣称与石化工艺相比,生物工艺的成本将降低30%。相关产品的成功展示了绿色生物制造二元胺和醇的技术经济可行性和巨大的应用前景。
然而,对于绝大多数二元胺和二元醇的生物合成仍存在众多挑战,如大多数的生物合成成本仍无法满足工业需要;自然界中缺乏1,5-戊二醇等二元醇的天然生物合成路径;二元胺主要采用精氨酸、鸟氨酸和赖氨酸等氨基酸为原料的全细胞催化工艺,脱羧造成CO2排放无法利用等。因此,开发以非粮生物质和一碳原料等可再生原料生产二元胺和醇的生物合成路线和发酵工艺,是近年关注的研究重点,对于降低化石资源依赖、减少CO2的排放、降低成本、推动生物基二元胺和醇的规模化生产具有重要的意义。
脂肪族短链二元胺和醇常用化学合成法和生物合成法的对比
近年来,合成生物学、代谢工程、生物信息学的飞速发展不断为可再生原料的利用,生物合成脂肪族短链二元胺和醇带来新的进展。本文针对利用可再生原料生物合成短链二元胺1,3-丙二胺、1,4-丁二胺、1,5-戊二胺,以及短链二元醇1,3-丙二醇、1,4-丁二醇、1,5-戊二醇的研究进展,概况了可再生原料生物制造的碳循环和代谢途径,总结了短链二元胺和醇的从头生物合成路线,阐述了利用木质纤维素水解糖、粗甘油、一碳化合物原料合成短链二元胺和醇的研究现状,并对脂肪族短链二元胺和醇生物制造的主要挑战进行了相关讨论和展望。
01 可再生原料生物制造的碳循环和代谢途径
利用可再生原料生产燃料、化学品驱动了工业生物技术发展。生物质是含碳的可再生原料,主要来自于农业、林业和工业等领域,可分为木质纤维素生物质、林业生物质、农业生物质和废弃物生物质。纤维素、半纤维素、木质素、淀粉、糖、油脂等是生物质原料的基本成分。目前各种生物质原料已被广泛应用于生物炼制,见图1。第一代生物炼制,主要以粮食作物生物质为原料。随着全球面临粮食危机,“不与人争粮,不与粮争地”原则推动了第二代以木质纤维素等非粮生物质为原料的生物炼制。CO2排放不断增加导致全球变暖等诸多环境问题引起全球关注,越来越多的研究转向第三代生物炼制。直接以CO2和其衍生的一碳化合物,如甲烷、甲醇、甲酸等为原料,可进一步降低原料成本,减少对粮食依赖,推进生物制造低碳、绿色、可持续发展。
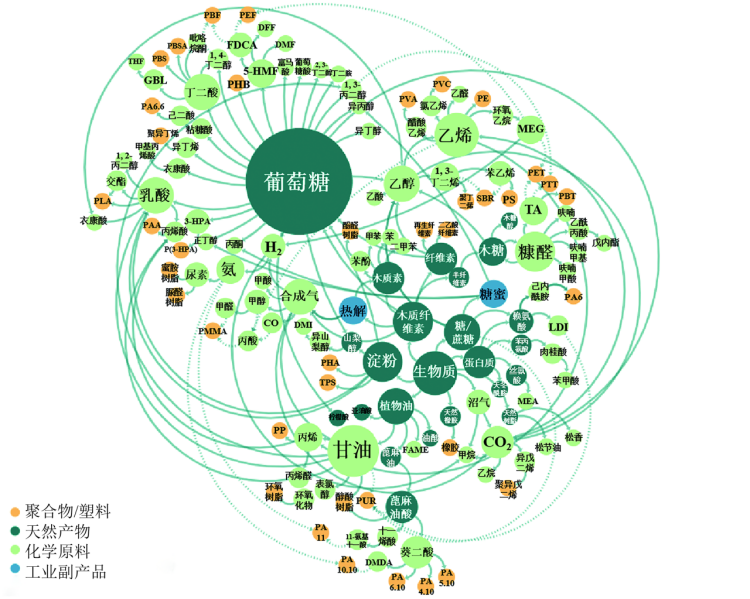
图1 生物质原料和产品图
以木质纤维素、粗甘油等非粮生物质以及CO2和其衍生的一碳化合物为原料生物合成短链二元胺和醇,可以促进来自农业、林业和工业的废弃物的有效利用,建立基于CO2的碳生物循环(图2)是生物基材料的可持续发展重要一环,对促进低经济转型和解决环境问题具有至关重要的作用。目前,关于木质纤维素水解糖、甘油、一碳化合物的代谢已被报道有多种微生物具有相关的代谢途径。
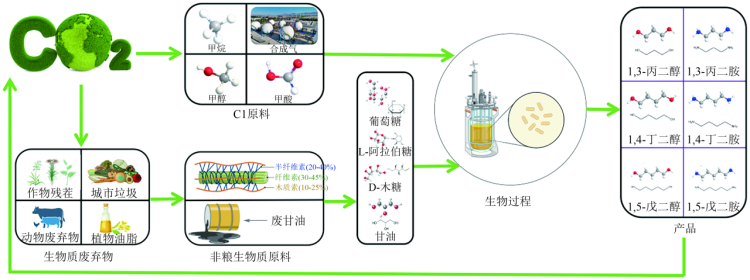
图2 脂肪族二元胺和二元醇生物制造的碳经济循环示意图 1.1 木质纤维水解糖类的代谢途径
木质纤维素生物质主要来源于农作物秸秆等农业废弃物、木材废料等森林废弃物等,全球产量巨大,每年约1800亿吨。木质纤维素生物质主要由纤维素、半纤维素和木质素构成,其水解产物包含葡萄糖、半乳糖等己糖,以及木糖、阿拉伯糖等戊糖的混合物,其中葡萄糖占比60%~70%,其余为D-木糖、L-阿拉伯糖等非葡萄糖糖类,因此是许多生物基产品理想的原料。研究发现,木糖、阿拉伯糖可以被细菌、酵母等多种微生物代谢利用并具有相似的代谢途径,包括基于磷酸化的代谢途径和非磷酸化途径。磷酸化的代谢途径中木糖和阿拉伯糖可经异构酶途径或还原酶-脱氢酶途径合成木酮糖-5-磷酸,而后通过磷酸戊糖途径(PPP)进入中心碳代谢。非磷酸化途径中则通过一系列脱氢酶、内酯酶和脱水酶催化作用下分别合成2-酮-3-脱氧木糖酸和2-酮-3-脱氧阿拉伯糖酸,随后进入中心碳代谢。
1.2 甘油代谢途径
粗甘油在工业领域中是生产生物柴油酯交换过程中主要废弃物,其过剩的积累导致环境问题。开发低成本粗甘油的利用势在必行。甘油是微生物生长的重要底物之一,梭菌属(Clostridium)、乳酸菌属(Lactobacillus)、克雷伯氏菌属(Klebsiella)等都具有代谢甘油的途径,主要分为氧化途径和还原途径。在厌氧和微氧情况下,甘油可以经甘油脱水酶和1,3-丙二醇氧化还原酶/1,3-丙二醇脱氢酶两步催化、还原生成1,3-丙二醇。该途径不产生能量,同时需要消耗还原力。甘油的氧化途径则分为脱氢途径和磷酸化途径,甘油通过一系列反应进入糖酵解途径和三羧酸循环(TCA)产生能量和还原力。
1.3 一碳化合物代谢途径
化石资源的使用造成大量CO2的排放,根据国际能源署《2023年的二氧化碳排放量》报告,2023年,全球与能源相关的二氧化碳排放量增长1.1%,增加4.1亿吨,达到374亿吨的历史新高。 目前,在自养微生物、硫酸盐还原菌等生物体内发现了7条天然CO2固定途径,分别为Wood Ljungdahl途径、卡尔文循环、还原三羧酸循环途径、二羧酸/4-羟基丁酸循环、3-羟基丙酸循环、3-羟基丙酸/4-羟基丁酸循环和还原甘氨酸途径。其中Wood Ljungdahl途径和还原甘氨酸途径属于线性固碳途径。Wood Ljungdahl途径分为两个支路:一分子CO2经甲基支路一系列酶催化作用将甲基转移到乙酰CoA合酶;另一分子CO2通过羟基支路经CO脱氢酶催化生成CO,并与甲基支路上甲基和乙酰CoA在乙酰CoA合酶作用下合成乙酰CoA。还原甘氨酸途径常被用于模式微生物中构建CO2和甲酸的同化途径,甲酸经过还原和环化形成5,10-亚甲基四氢叶酸,然后经核心固碳酶甘氨酸裂解体系(glycine cleavage system,GCS)催化固定CO2生成甘氨酸。卡尔文循环可分为三个阶段:①羧化,核酮糖-1,5二磷酸(RuBP)在核酮糖-1,5二磷酸羧化酶/加氧酶(RuBisCO)的作用下与CO2缩合并分解为2分子3-磷酸甘油酸;②还原,3-磷酸甘油酸磷酸化形成1,3-二磷酸甘油酸,再还原形成3-磷酸甘油醛;③RuBP再生,3-磷酸甘油醛经过一系列反应转变为5-磷酸核酮糖,再由磷酸核酮糖激酶(PRK)催化进行磷酸化形成RuBP。其余还原三羧酸循环途径、二羧酸/4-羟基丁酸循环、3-羟基丙酸循环和3-羟基丙酸/4-羟基丁酸循环均是利用乙酰CoA和琥珀酰CoA之间的循环实现固碳。 CO2经加氢、光/电催化等可合成甲烷、甲酸、甲醇等一碳化合物,这些一碳化合物在生物体内代谢分为氧化途径和同化途径。氧化途径主要通过一系列氧化酶将高还原态的一碳化合物氧化最终生成CO2,为细胞提供能量和还原力。同化途径主要分为包括卡尔文循环、还原型乙酰CoA途径、乙醛酸再生途径、一磷酸核酮糖途径、丝氨酸途径、还原型乙酰CoA途径和一磷酸木酮糖途径。能够通过自身代谢利用一碳化合物作为唯一碳源和能源进行生长的微生物统称甲基营养型微生物,大致可分为天然型和合成型微生物两类。天然甲基营养型微生物可以通过自身的代谢途径实现对C1化合物的利用,而合成甲基营养型微生物是结合丰富的基因编辑手段,改造模式微生物,如大肠杆菌、谷氨酸棒状杆菌和酿酒酵母,使其利用一碳化合物高效生产目标产物。姚伦等和郭姝媛等对相关途径和微生物进行了详细的阐述。
02 脂肪族短链二元胺和醇的从头生物合成路线
从头生物合成途径的建立对脂肪族短链二元胺和醇的生物合成起到决定性作用。其生物合成主要可以通过糖酵解途径、三羧酸(TCA)循环和氨基酸合成途径合成关键的核心前体,进而延伸到氨基酸等前体物质的分解代谢途径合成1,3-丙二胺、1,4-丁二胺、1,5-戊二胺、1,3-丙二醇、1,4-丁二醇、1,5-戊二醇,见图3。
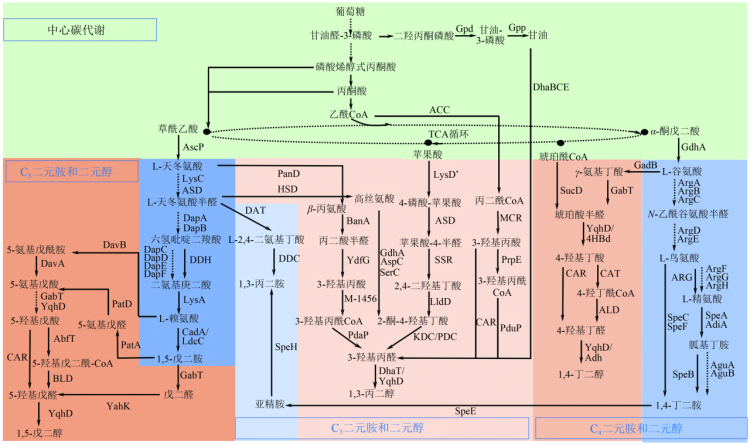
图3 脂肪族短链二元胺和二元醇从头合成途径示意图 2.1 1,3-丙二胺和1,3-丙二醇的从头生物合成路线
1,3-丙二胺是一种三碳主链的二元胺,可用于合成聚酰胺、药物、农用化学品等。目前,1,3-丙二胺的生物合成路线以L-天冬氨酸、L-谷氨酸为关键前体氨基酸,分别通过TCA循环的α-酮戊二酸(α-KG)经谷氨酸脱氢酶(GDH)转化合成L-谷氨酸(C5途径),或草酰乙酸(OAA)经天冬氨酸转氨酶(AspC)转化生成L-天冬氨酸(C4途径)。C5途径以L-谷氨酸为前体经精氨酸合成途径合成L-精氨酸,进而在精氨酸脱羧酶(SpeA)、胍基丁胺脲水解酶(SpeB)、亚精胺合成酶(SpeE)和亚精胺脱氢酶(SpdH)的作用下经1,4-丁二胺合成1,3-丙二胺。C4途径则是以L-天冬氨酸为前体生成天冬氨酸半醛,进而在2-酮戊二酸-4-氨基转移酶(DAT)、L-2,4-二氨基丁酸酯脱羧酶(DDC)的催化作用下合成1,3-丙二胺。在Pseudomonas aeruginosa和Acinetobacter baumannii中分别通过C5途径和C4途径合成1,3-丙二胺,但产量均较低。Chae等分析对比了C4和C5途径,选择了效率更高的Acinetobacter baumannii的C4途径在大肠杆菌中异源构建,并进一步过表达了ppc和aspC基因,敲除pfkA促进1,3-丙二胺合成,最后通过分批发酵产生了13g/L的1,3-丙二胺。随后的多项研究针对C4途径的关键酶进行挖掘和筛选。 1,3-丙二醇是制备聚对苯二甲酸丙二醇酯的关键单体,也可作为有机溶剂广泛应用。从葡萄糖可通过高丝氨酸衍生途径、3-羟基丙酸衍生途径、丙二酰CoA衍生途径和苹果酸衍生途径合成1,3-丙二醇。高丝氨酸衍生途径和3-羟基丙酸衍生途径均以L-天冬氨酸为氨基酸前体。高丝氨酸衍生途径首先在天冬氨酸激酶、天冬氨酸半醛脱氢酶、高丝氨酸脱氢酶催化作用下合成高丝氨酸,而后在经2-酮-4-羟基丁酸中间体合成为3-羟基丙醛,最后在醇脱氢酶(DhaT)作用下合成1,3-丙二醇。3-羟基丙酸衍生途径首先通过L-天冬氨酸-α-脱羧酶(PanD)、β-丙氨酸丙酮酸转氨酶和丙二酸半醛还原酶催化作用下合成3-羟基丙酸,最后利用3-羟基丙酰CoA合酶、醛脱氢酶和醇脱氢酶合成1,3-丙二醇。丙二酰CoA衍生途径则是乙酰CoA经丙二酰CoA合成3-羟基丙酸,最后合成1,3-丙二醇。苹果酸衍生途径通过苹果酸前体经苹果酸激酶(LysD)、苹果酸半醛脱氢酶(ASD)和醛脱氢酶(SSR)催化生成2,4-二羟基丁酸,进一步经氧化生成2-酮-4-羟基丁酸,在α-酮酸脱羧酶(KDC/PDC)作用下将2-酮-4-羟基丁酸转化为3-羟基丙醛而后合成1,3-丙二醇。杜邦公司则开发了生物催化剂以葡萄糖合成1,3-丙二醇的路线,产量达135g/L,收率3.5g/g,实现了1,3-丙二醇的商业化生产。
2.2 1,4-丁二胺和1,4-丁二醇的从头生物合成路线
1,4-丁二胺是一种广泛存在于许多植物、动物和微生物中的二元胺,可用于制备橡胶硫化促进剂和聚酰胺材料,作为关键单体聚合制备的尼龙46和其他高温尼龙性能优良,应用广泛。目前存在三种1,4-丁二胺的生物合成路径,分别是广泛存在于微生物体内的鸟氨酸脱羧酶(ODC)路径、精氨酸脱羧酶(ADC)路径以及动植物细胞内的精氨酸酶(ARG)路径。三条途径均首先经中间体α-KG生成L-谷氨酸,而后在N-乙酰谷氨酸合酶(ArgA)或鸟氨酸乙酰转移酶(ArgJ)、N-乙酰谷氨酸激酶(ArgB)、乙酰谷氨酰半醛脱氢酶(ArgC)、乙酰鸟氨酸转移酶(ArgD)和乙酰鸟氨酸脱乙酰基酶(ArgE)的级联催化下生成L-鸟氨酸。直接发酵法合成1,4-丁二胺的研究工作主要集中在ODC路径,即L-鸟氨酸经鸟氨酸脱羧酶(SpeC或SpeF)脱羧合成1,4-丁二胺。ADC路径和ARG路径则是继续由鸟氨酸氨基甲酰基转移酶(ArgF)、精氨酸琥珀酸合成酶(ArgG)、精氨酸琥珀酸裂解酶(ArgH)的催化作用下合成L-精氨酸前体,而后ADC路径在精氨酸脱羧酶和胍丁胺酶作用下将L-精氨酸催化合成1,4-丁二胺;ARG路径则是精氨酸酶(ARG)和鸟氨酸脱羧酶作用下合成1,4-丁二胺。Lee研究团队选择同时具有ODC和ADC途径的大肠杆菌作为底盘细胞,通过敲除基因argI、speE、speG、puuA、puuP减少前体鸟氨酸和1,4-丁二胺的消耗;利用启动子调控argE、argCBH和speC基因强化合成,同时解除反馈调节,通过葡萄糖分批补料发酵合成了24.2g/L的1,4-丁二胺,生产速率为0.75g/(L·h)。随后,利用sRNA微调1,4-丁二胺合成相关基因的表达,结合通量响应分析和计算机代谢模拟选择靶基因,在弱启动子表达sRNA情况下,降低argF基因和glnA基因的表达,可合成42.3g/L的1,4-丁二胺,生产速率是1.26g/(L·h),为目前报道大肠杆菌发酵法最高产量。 1,4-丁二醇作为关键材料单体用于合成聚对苯二甲酸丁二酯(PBT)、聚丁二酸丁二酸酯(PBS)、聚丁二酸丁二酸酯(PBSA)等,其合成的聚酯材料年产量可达到250×104t,市值61.9×108USD。1,4-丁二醇合成途径主要分为α-KG衍生途径和琥珀酰CoA衍生途径。α-KG衍生途径与1,4-丁二胺合成途径的前体相同,即首先α-KG生成L-谷氨酸,再经由谷氨酸脱羧酶(GadB)、转氨酶(GabT)合成琥珀酸半醛,醇脱氢酶催化随即生成4-羟基丁酸,然后可通过羧酸还原酶(CAR)一步或者在4-羟基丁酸辅酶A转移酶(CAT)和醛脱氢酶(ALD)两步催化合成4-羟基丁醛,最后4-羟基丁醛通过醛还原酶(YqhD)或醇脱氢酶(Adh)生成1,4-丁二醇。琥珀酰CoA衍生途径是TCA循环中间体琥珀酰CoA经琥珀酸半醛脱氢酶(SucD)催化合成琥珀酸半醛,然后同上述途径经琥珀酸半醛生成1,4-丁二醇。自然界中没有天然的1,4-丁二醇合成途径,Yim等通过计算机辅助途径设计与基因组尺度的代谢模型相结合,成功开发了琥珀酰CoA衍生途径合成1,4-丁二醇,将其构建于大肠杆菌中并采用多项策略进行系统改造优化。其开发的工艺利用葡萄糖可生产125g/L的1,4-丁二醇,收率达到0.4g/g,由Genomatica公司成功实现商业化,并已授权多家公司生产,产能已超10×104t/a。
2.3 1,5-戊二胺和1,5-戊二醇的从头生物合成路线
1,5-戊二胺是合成尼龙5X的关键单体,其生物合成路线首先合成L-赖氨酸前体。葡萄糖经OAA合成L-天冬氨酸,L-天冬氨酸再通过二氨基庚二酸(DAP)途径合成赖氨酸。此过程在不同生物体内可分为两种:一是经过2,3,4,5-四氢吡啶-2,6-二羧酸N-琥珀酰转移酶(DapD)、琥珀酰二氨基庚二酸转氨酶(DapC)、琥珀酰二氨基庚二酸脱琥珀酰基酶(DapE)、二氨基庚二酸差向异构酶(DapF)一系列酶催化,将六氢吡啶二羧酸合成二氨基庚二酸;二是通过二氨基庚二酸脱氢酶(DDH)一步催化,将六氢吡啶二羧酸合成为二氨基庚二酸,随后通过二氨基庚二酸脱羧酶(LysA)催化合成赖氨酸。最后在赖氨酸脱羧酶(CadA/LdcC)作用下生成1,5-戊二胺。Kim等通过代谢工程改造用于赖氨酸生产的谷氨酸棒杆菌,采用强启动子异源表达来源于大肠杆菌的LdcC,以葡萄糖为原料补料分批发酵合成103.78g/L的1,5-戊二胺。在此基础上进一步筛选了不同来源的LdcC,采用强启动子整合表达Hafnia alvei来源的LdcC后1,5-戊二胺提高为125g/L,为目前报道发酵合成的最高产量。 1,5-戊二醇作为一种重要单体可用于合成聚酯、塑料、纤维等高分子材料。1,5-戊二醇缺乏天然合成途径,目前报道了四条L-赖氨酸衍生的人工合成途径。主要是赖氨酸为前体利用赖氨酸单加氧酶(DavB)和5-氨基戊酰胺酶(DavA)合成5-氨基戊酸,然后在转氨酶(GabT)和醇脱氢酶(YqhD)催化下合成5-羟基戊酸,再经由羧酸还原酶(CAR)一步催化或经5-羟基戊二酰-CoA还原两步催化合成5-羟基戊醛,最后通过醇脱氢酶合成1,5-戊二醇。此外,1,5-戊二醇还可以1,5-戊二胺为前体,通过戊二胺转氨酶(PatA)和戊二醛脱氢酶(PatD)将戊二胺转化为5-氨基戊酸,进而同上述途径合成1,5-戊二醇。2024年,Hua等报道了一条由戊二胺经转氨酶连续转氨生成戊二醛,再通过醇脱氢酶还原生产1,5-戊二醇的新路径。目前,1,5-戊二醇的生物合成产量还相对较低。Cen等在大肠杆菌中构建经5-羟基戊二酰-CoA合成的1,5-戊二醇途径,合成了0.12g/L的1,5-戊二醇。1,5-戊二胺衍生的1,5-戊二醇合成途径具有较高的理论产率和催化效率,报道最优工程菌株分批补料发酵生产9.25g/L的1,5-戊二醇,产率为0.28mol/mol葡萄糖。
03 木质纤维素水解糖原料合成脂肪族短链二元胺和醇
木质纤维素水解产物包含葡萄糖、木糖和阿拉伯糖等混糖。利用葡萄糖的同时,实现木糖、阿拉伯糖等其他糖类的有效利用,对于综合利用木质纤维素合成短链二元胺和醇至关重要,引起了广泛关注研究,见图4。
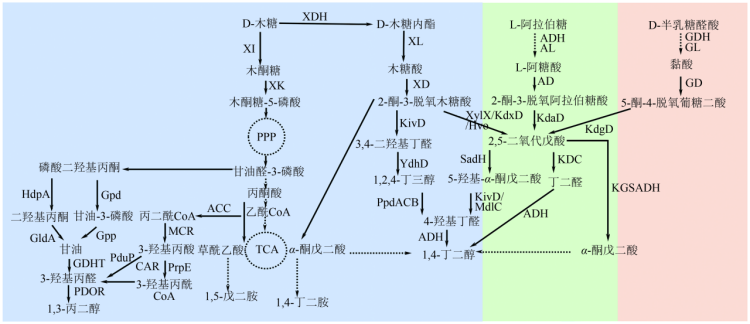
图4 木质纤维素水解糖原料合短链二元胺和二元醇途径
木质纤维素水解的D-木糖、L-阿拉伯糖等为原料合成1,4-丁二醇可避免以葡萄糖为原料的途径步骤冗长、代谢调控复杂等问题。Tai等在大肠杆菌中设计以D-木糖、L-阿拉伯糖和D-半乳糖醛酸为底物的1,4-丁二醇的合成途径,即经非磷酸化代谢途径的分别合成2-酮-3-脱氧木糖酸、2-酮-3-脱氧阿拉伯糖酸和5-酮-4-脱氧葡糖二酸,随后在相应脱氢酶、2-酮酸脱羧酶(KDC)和醇脱氢酶(ADH)的催化下合成1,4-丁二醇。该途径具有更简短的反应步骤,绕开TCA循环调控更加简单,优化后的大肠杆菌以D-木糖、L-阿拉伯糖和D-半乳糖醛酸为底物补料发酵分别生成12g/L、15.6g/L和16.5g/L的1,4-丁二醇。木糖在木质纤维素中的含量仅次于葡萄糖。围绕木糖为原料开发设计了多条1,4-丁二醇的人工合成路径。Liu等设计的路线通过6个催化步骤,即D-木糖脱氢酶、D-木酮酸脱水酶、2-酮-3-脱氧-D-木酮酸脱水酶、酮酸脱羧酶和两步醇脱氢酶(SADH和ADH)催化,将木糖转化合成1,4-丁二醇,优化后产量为0.44g/L,产率0.07mol/mol。Wang等则针对其中副产物1,2,4-丁三醇积累的问题,设计利用二醇脱水酶(PpdACB)将1,2,4-丁三醇转化生成4-羟基丁醛,再通过醇脱氢酶合成1,4-丁二醇的途径,合成了1,4-丁二醇209mg/L。 由于甘油价格的波动,以木质纤维素为原料生产1,3-丙二醇得到了越来越多的关注。Li等在大肠杆菌中设计和构建了乙酰辅酶A衍生的1,3-丙二醇合成途径,通过引入丙二酰辅酶A依赖的3-羟基丙酸模块和筛选3-羟基丙酸转化合成1,3-丙二醇的关键酶,实现1,3-丙二醇的合成,利用20g/L木糖合成了0.82g/L的1,3-丙二醇,此外还考察了其以甘油和乙酸为原料合成1,3-丙二醇能力。随后,其在谷氨酸棒状杆菌中构建了甘油和1,3-丙二醇合成模块,并减少3-羟基丙醛积累,增加NADPH和ATP供给,以优化木糖代谢,成功实现同时利用葡萄糖和木糖生产1,3-丙二醇,产量达98.2g/L,产率0.38g/g。 利用木糖合成二元胺研究中,木糖异构酶(Ⅺ)途径是应用最广泛的木糖代谢途径。在谷氨酸棒状杆菌中构建Ⅺ途径并筛选木糖异构酶,可提高利用木糖合成1,4-丁二胺的生产速率和产量,达27.8mg/(L·h)和15.1mmol/L。在钝齿棒杆菌中构建XI途径并引入丁二胺合成途径实现木糖利用,通过RBS调控speB的表达水平,敲除snaA、speE和cgmR阻断丁二胺的降解,过表达转运蛋白CgmA等工程策略,最后利用葡萄糖和木糖混合糖以及模拟麦秸水解物分批补料发酵分别产生1,4-丁二胺36.8g/L和33.4g/L,产率为0.15g/g和0.14g/g。Buschke等在谷氨酸棒状杆菌中通过构建XI途径实现了利用木糖合成14mmol/L的1,5-戊二胺,进一步利用半纤维素水解液产生20mmol/L的1,5-戊二胺。随后在此基础上利用组学分析靶点后进行系统代谢工程改造谷氨酸棒状杆菌,提高了利用木糖合成1,5-戊二胺的产量,通过补料发酵产量达103g/L,产率32%。Imao等利用代谢工程技术和细胞表面展示技术实现了直接以低聚木糖为原料,通过构建Ⅺ途径实现谷氨酸棒状杆菌对木糖的利用,并将来源于枯草芽孢杆菌的β-木糖苷酶BSU17580利用PorH锚定蛋白在谷氨酸梭菌细胞表面表达将低聚木糖转化成木糖,进而结合赖氨酸脱羧酶合成1,5-戊二胺,最终产生11.6mmol/L的1,5-戊二胺。此外,选择具备天然木糖代谢途径的宿主也是实现木糖高效利用合成二元胺的有效策略。Li等选择具有高效利用木糖能力的Bacillus amyloliquefaciens,通过代谢工程改造1,4-丁二胺的合成模块、NADPH合成和ATP供给模块,实现利用木糖合成5.51g/L的1,4-丁二胺,产率0.14g/g,利用五节芒水解液可合成6.76g/L的1,4-丁二胺。
04 粗甘油原料合成脂肪族短链二元胺和醇
微生物对甘油具有良好的利用能力,目前粗甘油已被广泛用作替代原料合成化学品。利用甘油生物合成1,3-丙二醇的途径简单,仅需两步催化反应,是其理想的原料之一。克雷伯氏菌属、梭菌属等多种微生物均具备直接以甘油为原料合成1,3-丙二醇的能力,得到了广泛研究。 Klebsiella pneumoniae DSM 4799利用粗甘油可生产80g/L的1,3-丙二醇,并进一步采用固定化细胞分批重复投料发酵形式,可减缓粗甘油发酵时杂质积累的抑制情况。针对1,3-丙二醇规模化生产过程中副产物乳酸积累问题,Xu等将K. pneumoniae LDH526的乳酸脱氢酶基因ldhA敲除提高1,3-丙二醇生产性能,产量、产率和生产速率分别达102.06g/L、0.52mol/mol和2.13g/(L·h)。Clostridium butyricum AKR102a在1,3-丙二醇合成中展现了良好的耐受性和生产性能,以纯甘油和粗甘油为原料1,3-丙二醇的生产速率分别可达3.3g/(L·h)和2.3g/(L·h),产量为93.7g/L和76.2g/L。Clostridium strain BOH3利用甘油可合成103.55~116.35g/L的1,3-丙二醇。此外,Lactobacillus diolivorans DSM14421、Clostridium diolis DSM15410以及微生物菌群等都展现了优良的以甘油为原料合成1,3-丙二醇的能力。 另外,采用非天然的1,3-丙二醇生产菌株作为底盘细胞进行代谢工程改造也是实现利用甘油生产1,3-丙二醇的有效手段。将来源于丁酸梭菌的甘油脱水酶基因dhaB1和它的激活因子基因dhaB2与大肠杆菌的醇脱氢酶基因yqhD引入Escherichia coli K-12 ER2925中构建1,3-丙二醇合成途径,同时利用温度启动子控制采用两段工艺合成1,3-丙二醇,产量和生产速率分别为104.4g/L和2.61g/(L·h)。利用Vibrio natriegens生长迅速,底物吸收能力强的优点,异源构建甘油合成1,3-丙二醇的途径实现69.5g/L的1,3-丙二醇合成。 此外,甘油也被证明是合成1,4-丁二醇的有效原料。Liu等在大肠杆菌中组装琥珀酰CoA衍生的1,4-丁二醇合成途径,采用基因工程和生物过程策略优化,分别以纯甘油和粗甘油为底物生产1,4-丁二醇达到1.31g/L和1.07g/L,分批补料发酵,1,4-丁二醇提高到5.75g/L,产率为143.75mg/g。 以甘油为原料生物合成二元胺的研究较少,Meiswinkel等在谷氨酸棒状杆菌中表达来源于大肠杆菌的甘油激酶(glpK)、甘油-3-磷酸脱氢酶(glpD)和甘油孔蛋白基因(glpF),成功利用20g/L甘油合成4.9mmol/L的1,4-丁二胺,产率0.02g/g;增加10mmol/L葡萄糖采用混碳源模式可合成9.7mmol/L的1,4-丁二胺。
05 一碳化合物原料合成脂肪族短链二元胺和醇 5.1 一碳化合物为生物合成原料
“双碳”目标下,一碳化合物的高效利用成为研究热点。一碳化合物来源广泛、制备容易、价格低廉,是理想的新一代原料。在脂肪族短链二元胺和醇生物合成过程中利用CO2、甲烷、甲醇的研究取得了一定的进展,目前具备一碳化合物代谢能力的微生物是实现生产的主力。自养生物Chlamydomonas reinhardtii中1,4-丁二胺占总细胞干重的0.3%,被认为是生产多元胺理想的宿主之一。利用其天然优势,通过筛选不同来源的鸟氨酸脱羧酶,表达精氨酸酶,提高前体可用性以及功能性敲除产物降解途径基因,使得利用CO2合成1,4-丁二胺的产量提高10倍,得到200mg/L的1,4-丁二胺。甲烷氧化菌Methylomicrobium alcaliphilum 20Z可以利用甲烷作为唯一碳源和能源,通过适应性进化提高细胞对1,4-丁二胺的耐受性,然后经一系列改造优化,包括表达异源鸟氨酸脱羧酶基因speC,过表达argJ和argD,敲除speE、ack和ldh基因,使利用甲烷合成1,4-丁二胺产量提高了近8倍,达到98.08mg/L。采用甲基营养型细菌Bacillus methanolicus为宿主,异源表达两种赖氨酸脱羧酶cadA和ldcC基因,实现了从甲醇到1,5-戊二胺的生物合成,摇瓶和高密度甲醇发酵分别生产得到300mg/L和6.5g/L的1,5-戊二胺。同样在甲烷氧化菌中异源表达两种赖氨酸脱羧酶也可以实现由甲烷生物合成0.289g/L的1,5-戊二胺。 一碳化合物在脂肪族短链二元醇的合成方面目前主要围绕1,3-丙二醇。Hirokawa等利用工程蓝藻直接从二氧化碳生产1,3-丙二醇,在Synechococcus elongatus PCC 7942引入合成代谢途径产生了3.48mmol/L的1,3-丙二醇和14.3mmol/L的甘油。随后通过计算机模拟筛选干扰基因,优化后1,3-丙二醇的合成产量提高到4.44mmol/L。针对甘油积累过多的问题,采用强的启动子增强甘油转化为1,3-丙二醇的基因,并结合条件优化,将1,3-丙二醇的产量提高到16.1mmol/L。Liu等则在Anabaena PCC7120中构建了一条异源合成途径,直接利用CO2和太阳能合成1,3-丙二醇46.0mg/L。Meng等在大肠杆菌中设计构建了一条以甲醛和乙醇为底物利用脱氧核糖-5-磷酸醛缩酶合成1,3-丙二醇的新途径,并通过删除转化甲醛的frmA基因,1,3-丙二醇的产量最初的5.67mmol/L提高到17.35mmol/L,产率0.057mol/mol提高到0.096mol/mol。
5.2 CO2原位循环固定利用
生物合成二元胺和二元醇过程中,通常会产生CO2导致碳损失,如1,3-丙二醇合成途径产生的CO2和其他副产物导致损失30%~50%的碳,1,5-戊二胺合成中的脱羧反应导致每生成1mol产物同时伴随生产1mol CO2。将CO2原位循环固定可有效减少CO2排放并提高原子的利用效率。南京工业大学Chen团队在生产1,5-戊二胺的大肠杆菌中异源表达RuBisCO和PRK,构建RuBisCO分支,实现CO2的原位固定,基于化学计量网络模型模拟和通量模型分析显示引入RuBisCO分支后,1,5-戊二胺产率可从0.45g/g可提高至0.47g/g。随后利用启动子优化CO2固定模块与ATP供应模块、自组装蛋白支架系统优化代谢途径,最优工程菌株在5L生物反应器中分批发酵,1,5-戊二胺产量和产率分别达到84.1g/L和0.37g/g葡萄糖。此外,还基于脱羧CO2设计1,5-戊二胺和丁二酸的联产体系,将CO2的原位供给厌氧合成丁二酸的途径,同时利用1,5-戊二胺和丁二酸的酸碱特性进行pH中和,减少酸碱用量和CO2排放,且1,5-戊二胺丁二酸盐可用于合成PA54。
06 结语和展望
在“双碳”目标下,采用可再生原料生物合成二元胺和二元醇实现碳循环可有效减少碳排放和原料成本。目前,脂肪族短链二元胺和醇的生物合成途径已建立并用于开发利用多样化可再生原料,但仍存在诸多挑战。 (1)原料成本占比大。生物基1,3-丙二醇和1,4-丁二醇虽然实现了规模化生产,但仍需降低生产成本以进一步推动其大规模商业化应用,其中原料成本占比较大(25%~50%),利用更廉价的原料无疑是降低成本拓展大规模应用的关键。虽然目前已成功实现了木糖、甘油乃至以一碳化合物原料的利用,但是产量相对较低。因此,强化非粮生物质和一碳化合物的利用途径,开发多样化原料共利用代谢工程策略,缓解木质纤维素水解液、粗甘油等对细胞的毒害是充分利用低劣生物质、提高产量的关键之一。 (2)生产效率无法满足工业生产的需求。虽然已经建立发酵直接生产1,4-丁二胺、1,5-戊二胺、1,5-戊二醇的方法,但产率和产量较低。因此,一方面需要针对羧酸还原酶、转氨酶等关键限速酶采用蛋白质工程改造提高酶的专一性和催化活性,提高途径的效率;另一方面,亟需挖掘、开发更多高效新途径,以满足工业生产需求。 (3)合成过程中还原力的需求。脂肪族短链二元胺和醇是还原性化合物,生物合成过程中需要大量的还原力。还原力不足不仅会导致产品产率低的问题,还会使原料分流氧化途径产生还原力,同时伴随乳酸、乙酸、乙醇等多种副产物的产生。研究人员目前通过调控氧化还原力平衡、碳流的精准重新分配、平衡氧化和还原途径等多种策略调控胞内还原力。此外,电发酵利用清洁电能将胞外电子转化成胞内的还原力NAD(P)H也为生物合成二元胺和二元醇提供了一种新还原力供给策略。 综上,得益于合成生物学、代谢工程、生物信息学、人工智能的快速发展,有望创制高效的二元醇和二元胺的生物合成工艺和细胞工厂,实现非粮生物质、一碳化学物等原料的综合利用,推动生物基材料领域的发展。 ▌参考信息:本文部分素材来自化工进展。由作者重新编写,系作者个人观点,本平台发布仅为了传达一种不同观点,不代表对该观点赞同或支持。如果有任何问题,请联系我们:15356747796(微信同号)




