上海交大倪俊组:化学酶平台新策略用于木质素到分子的高效转化
木质素价值化对于实现经济可行和可持续的木质纤维素生物精炼厂至关重要。近年来,木质素及其水解芳烃的生物利用引起了广泛关注,这是实现零浪费和经济可行的生物精炼厂的关键。然而,对昂贵辅因子(例如,三磷酸腺苷(ATP)、还原烟酰胺腺嘌呤二核苷酸磷酸(NADPH)和辅酶 A (CoA))的持续需求严重阻碍了木质素可持续地转化为有价值的产品。为了减轻这种限制,一种可能的方法是引入辅助辅因子再生酶,这通常需要精确调节辅因子代谢网络以防止细胞稳态的破坏。
此外,生物合成机械和辅因子再生系统之间催化活性的不平衡是有效转化的关键障碍,导致木质素有价值的分子的产量极其有限。例如,来自木质素衍生的对香豆酸(pCA)的覆盆子酮(RK)的生产率低于 0.003 g l−1h−1,转化率仅为 11.3%,姜黄素的生产率限制为 0.006 gl−1h−1。
目前,没有通用的解决方案可以同时克服昂贵的辅因子需求和不平衡的酶活性。因此,开发一种改善木质素生物转化途径的通用策略是可取的。
【SynBioCon】获悉,上海交通大学倪俊团队于2025年5月在期刊《Nature Synthesis》上发表了题为“ Chemoenzymatic platform with coordinated cofactor self-circulation for lignin valorization”的文章,报告了一种体外多酶协同表达与辅因子自循环(iMECS)策略,以实现木质素到分子的高效转化。

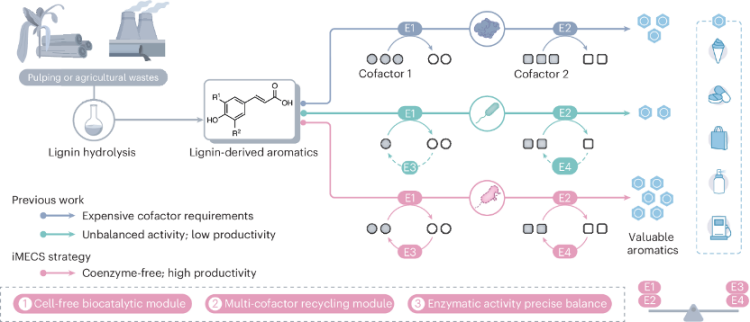
该文章展示了一种广泛适用的策略,该策略将辅酶再生和无细胞表达无缝集成到木质素升级过程中,称为体外多酶协调表达与辅因子自循环(iMECS)策略(图1)。木质素到分子的转化管道分为三个主要步骤:(1)为无细胞生物催化模块选择合适的酶,(2)构建多辅因子回收模块和(3)微调 DNA 添加以实现酶活性的精确平衡。
在这项研究中,研究者使用自动化液体处理工作流程快速筛选了1,296个独特的途径组合和20多个反应组分组,将姜黄素生产率提高到 0.175 gl−1h−1,摩尔收率为 95.31%,还展示了 iMECS 平台的灵活性。在没有添加外部辅助因子的情况下,基于iMECS 的路线的整体催化效率提高了48倍。
接下来,实施了串联化学解聚和无辅酶生物转化工艺,直接从富含木质素的农业废弃物中生产有价值的芳烃。这种具有非凡效率的通用可持续系统对于木质素增值非常可行,这促进了下一代生物精炼厂的经济可行性。
研究结果与讨论:
1、木质素-分子途径的多维优化
为了评估 iMECS 策略的可行性,研究者选择了姜黄素。它是由阿魏酸合成的,阿魏酸是一种主要的木质素单体,通过将对香豆酸-CoA连接酶(4CL)与姜黄素类合酶(CUS)偶联而合成。首先,研究者建立了一个生物催化模块,由拟南芥的4CL和水稻的CUS组成,并充分添加必要的辅因子(ATP、CoA和丙二酰辅酶A)以驱动生物合成路线。然而,在添加1mM阿魏酸的情况下,只合成了28.1 ± 2.9 mg/L姜黄素,并观察到阿魏酸的大量积累。因此,研究者研究了来自各种来源的阿魏酸转化替代酶。幸运的是,从Caldimonas热脱聚物中鉴定出阿魏酰辅酶A合成酶(FCS)姜黄素产量最高,为115.3±4.4mg/L。为了规避辅因子的消耗,他们还设计并引入了原位多辅因子回收模块,使用了丙二酰辅酶A合成酶(MatB)和多磷酸激酶2 III类(PPK)用于丙二酰辅酶A和ATP补充并同步回收CoA。四酶级联反应产生 126.4 mg/L的姜黄素,证明人工多辅因子回收模块成功循环了辅因子。然而,消除昂贵的纯化过程和提高整体效率仍然具有挑战性。
有了有效的多酶级联反应,研究者们着手建立一个iMECS系统,无需蛋白质纯化即可高效合成姜黄素。相应的姜黄素生产表明辅因子回收模块对姜黄素产量至关重要。有趣的是,在没有补充辅因子的情况下,辅因子再循环反应也产生了51.2 mg/L姜黄素,表明细胞裂解物中残留的辅因子足以启动iMECS系统。在PPK介导的系统中,ATP向一磷酸腺苷(AMP)的分布低于ATP 添加过多的系统中,这可能表明辅因子循环系统无法足够快地再生ATP以匹配姜黄素的生物合成。在这里,尽管 iMECS 策略在没有额外辅因子的情况下实现了姜黄素的合成,但转化率低。在牺牲底物浓度的第一层优化后,他们试图通过简单地调整每个质粒的比例来精确平衡酶活性。受体外原型设计和生物合成酶快速优化(iPROBE)工作流程的启发,研究者们通过将机器人液体处理系统与酶耦合生物传感器相结合来自动化 iMECS 框架,以加速优化过程。他们在一天内快速筛选了1,296个独特的途径组合,FCS:CUS:MatB:PPK 在 2:1:3:2 的负载比具有最高的姜黄素生产率,为 0.175 g L−1h−1,比全细胞生物转化高 1455% 以上。相应地,iMECS 系统对姜黄素的转化率达到 95.31%,远超以往研究报告的水平。这些数据证明了 iMECS 系统在快速建立木质素衍生分子转化的无辅酶途径方面的优越性。
2、用于高效合成香兰素的热稳定 iMECS
为了评估 iMECS 系统的广泛适用性,研究者们进一步探索了将阿魏酸转化为香兰素的催化过程。香兰素是一种广泛使用的风味化合物,FCS和烯酰辅酶A水合酶(ECH)负责这种转化:FCS 连接阿魏酸和乙酰辅酶A以形成阿魏酰辅酶 A,并消耗ATP,随后将阿魏酰辅酶A转化为香兰素和乙酰辅酶A。为了降低 ATP 需求,研究者们设计了一个由磷酸转乙酰酶(PTA)和乙酸激酶(ACK)组成的两步能量提取级联反应,作为 ATP 和 CoA 之间的“分子连接器”。具体来说,PTA 使用副产物乙酰辅酶A,同时产生的乙酰磷酸盐可以完美地被ACK用于ATP再生。另一种酶,聚磷酸盐AMP磷酸转移酶(PAP),负责能源和磷酸盐供应,被引入我们的设计中。使用全套五种纯化酶,辅因子成功循环以驱动 1 mM阿魏酸产生 94.4 ± 2.7 mg/L的香兰素。ATP 在五酶系统中向AMP的分布高于PPK介导的系统,这可能表明新构建的辅因子回收系统效率更高。在这里,五酶系统实现了香兰素的节能合成,与由 FCS 和 ECH 组成的双酶系统相比,能量提取级联理论上可以将 ATP 需求减少 67%。
接下来,研究者们尝试使用 iMECS 系统进一步优化香兰素的效率。对于初始阿魏酸的转化,使用FCS和ECH表达的无细胞双质粒系统,可产生 94.9 mg/L的香兰素。鉴于之前开发了一种温度导向的生物催化工艺来避免大肠杆菌全细胞催化中的副反应,通过高温(50 °C)灭活内源性 ADHs,而热稳定的外源酶可以保持其活性以完成催化合成。受这种方法的启发,我们提出一种基于温度的方法可以应用于无细胞系统。这种方法将在较高温度下使大肠杆菌提取物中存在的内源性嗜温酶失活,而表达的热稳定酶将保持活性。PTA、ACK 和 PAP 在 50℃下的热稳定性应满足温度导向策略的要求。由于获得了具有优异热稳定性的 CtFCS,我们推测CtFCS 基因下游的 CtECH 基因编码的 CtECH 可能是一个合适的候选者。事实上,具有更紧凑结构的CtECH 在 50 °C下相对稳定,孵育24小时后检测到约 60% 的初始活性,构建了用于FCS和ECH 表达的升级版无细胞双质粒系统。正如预期的那样,当反应温度从 30 °C 升高到 50 °C 时,获得了106.0mg/L香兰素,而没有可检测到的香草醇。通过进一步引入包含能量提取级联反应的辅因子回收模块,五质粒介导的热稳定 iMECS 系统合成了61.7 mg/L不添加辅因子的香兰素。随后,在 2:3:1:2:2 的优化 FCS:ECH:PTA:ACK:PAP 负载比下,香兰素的最高生产率达到 1.79 g L−1h−1,转化率从 44.05%提高到 98.21%。iMECS 系统的 pH 值在催化过程中保持相对稳定。总的来说,这些结果证明了 iMECS 系统在香兰素的无辅酶生物合成中的效率,并且本文描述的热稳定无细胞策略可广泛用于消除副产物。
3、三重辅因子循环促进 RK 生物合成
基于姜黄素和香兰素生物合成的结果,研究者们接下来的目标是证明 iMECS策略在更复杂的木质素到分子途径中的适用性。我们选择了从木质素衍生的 pCA 到 RK 的多辅因子依赖性途径作为模型。RK 途径可分为两个模块:上游4-羟基亚苄基丙酮(4HBA)合成模块和下游还原模块。由 FCS 和苯扎丙酮合酶(BAS)组成的上游模块类似于姜黄素生物合成途径,需要 ATP、CoA和丙二酰辅酶A作为辅助因子,下游模块涉及NADPH依赖性RK/zingerone合酶(RZS),它通过氧化还原机制将4HBA还原为 RK。首先,研究者们通过外部提供足够的辅因子,将上游模块与下游模块分开测试。由于 FCS 对 pCA 表现出优异的活性,因此我们使用无细胞双质粒表达系统筛选了可以提高 4HBA 滴度的 BAS。引人注目的是,来自Rhemu palmatum的 RpBAS 实现了 103.7 ± 4.9 mg /L的 4HBA 产量,比其他 BAS 高 2.2 倍)。接下来,他们尝试通过结合姜黄素生产中使用的多辅因子回收模块(MatB 和 PPK)来消除添加辅因子的需要。正如预期的那样,在 FCS、BAS、MatB 和 PPK 的体外蛋白质合成后,82.3 ± 5.8 mg/L的 4HBA 是在没有补充辅因子的情况下获得的,这意味着辅因子已成功循环以驱动上游模块。
为了构建下游模块,使用 CFPS 系统测试了来自不同来源的多个 RZS。来自大肠杆菌的 CurA(其中 CurA 是姜黄素还原酶)在 4HBA 还原中显示出最佳活性,RK 的滴度达到 141.8 ± 3.9 mg/L添加足够的 NADPH,甲酸盐脱氢酶(FDH)和葡萄糖脱氢酶(GDH)介导的系统与 CurA 催化途径显示出更好的相容性。考虑到不可逆的反应,我们使用了来自具有 D195Q/Y196R 突变的Candida boidinii 的 FDH34补充无细胞系统中的 NADPH。含有 CurA-FDH 双质粒系统的下游模块合成了 113.6 ± 4.0 mg/L的 RK。在 FDH 介导的系统中,NADPH 到 NADP 的分布低于过量的 NADPH 系统,这可能是其 RK 产量相对较低的原因。
接下来,研究者们着手建立一个 iMECS 系统,通过集成上下游模块来高效合成 RK。以前的研究表明,空间接近的融合酶可以提高级联效率,他们推测 CurA 和 FDH 的融合可以加速催化效率和辅因子再生。此外,融合策略可以降低 iMECS 系统的复杂性,以简化微调质粒添加的过程,这对于缺乏快速产品检测方法的系统尤为重要。在这里,与 GGGGS 接头的融合显示出更好的性能,我们进行了新一轮的组合测试以优化质粒添加比例。通过这些努力,在没有任何其他辅因子的情况下,采用 CurA-FDH 融合的 iMECS 系统达到 0.15 gL −1h−1的生产率,转化率为 91.56%。这比其他生物合成方法报告的产量高 48 倍。这些结果进一步证明了 iMECS 系统的优越性,该系统在从木质素衍生的芳烃合成更复杂的产品方面具有巨大潜力。值得注意的是,融合策略可能并不总是成功的。例如,尽管纯化的 FCS-BAS 融合性能优于单独的酶,当我们将 FCS 与 BAS 融合时,iMECS 的 RK 滴度降低了8.3倍。
综上所述,iMECS 策略提供了一个通用的无辅酶平台,用于将木质素有效转化为各种有价值的芳烃,从而促进可持续生物精炼厂的进一步发展。iMECS 介导的生物制造的一个主要好处是,使用富含木质素的农业废弃物作为原料,使生物制造与糖价脱钩。此外,木质素废物流的燃烧处理会释放大量 CO2,木质素回收不仅避免了这方面的碳排放,而且与传统的石油基芳烃合成相比,还减少了很大一部分温室气体排放。随着 CFPS 成本的不断降低,无细胞生产高价值靶标的可行性令人鼓舞。除了这些初步的概念验证演示外,我们还希望 iMECS 介导的平台能够提高下一代生物精炼厂的经济可行性。
https://www.nature.com/articles/s44160-025-00819-2
▌参考信息:本文部分素材来自公开资料。由作者重新编写,系作者个人观点,本平台发布仅为了传达一种不同观点,不代表对该观点赞同或支持。如果有任何问题,请联系我们:15356747796(微信同号)




